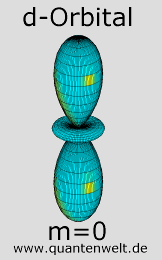









Eine weit verbreitete Möglichkeit, die d-Orbitale zu klassifizieren ist auf dieser Seite dargestellt. Die erste Abbildung zeigt das so genannte dz²-Orbital. Es ist mit dem Orbital mit der magnetischen Quantenzahl m=0 identisch. Die nächsten beiden Orbitale gehen aus den m=±1 Orbitalen hervor und bestehen jeweils aus vier Keulen, die zwischen der z-Achse und einer weiteren Achse des Koordinatensystems liegen. Man bezeichnet diese Orbitale als dxz- und dyz-Orbital. Die beiden weiteren d-Orbitale gehen werden aus den m=±2 Orbitalen gebildet. Eines hat vier Keulen, die zwischen der x- und der y-Achse liegen und heißt dxy-Orbital. Das andere liegt auf diesen Achsen und wird dx²y² genannt.
Diese Einteilung und Bezeichnung der Orbitale wird oft in der Chemie verwendet. Die Ausrichtung der Orbitalkeulen trägt bei der Bildung von Molekülorbitalen zur räumlichen Struktur der Moleküle bei.
d-Orbitale nach magnetischen Quantenzahlen
f-Orbitale nach magnetischen Quantenzahlen
f-Orbitale nach räumlicher Ausrichtung
Vergleich der ringförmigen Orbitale
Vergleich der keulenförmigen Orbitale
©1999-2025 Joachim Schulz - Nur echt auf www.Quantenwelt.de
Letzte Änderung: 28.03.2004